摘要:本研究突破傳統(tǒng)單因素病因框架,提出帕金森病(PD)的多維度發(fā)病機(jī)制。
當(dāng)談及帕金森病,人們往往會(huì)想到震顫、行動(dòng)遲緩等運(yùn)動(dòng)癥狀,但隱藏在這些表象之下的病因之謎卻一直困擾著科學(xué)界。這種神經(jīng)退行性疾病已成為全球增長最快的神經(jīng)系統(tǒng)疾病,預(yù)計(jì)到2040年患者人數(shù)將達(dá)到1750萬。傳統(tǒng)上,醫(yī)學(xué)界將帕金森病劃分為家族性和散發(fā)性兩種類型,然而這種非黑即白的分類方式正面臨挑戰(zhàn)——僅有10-15%的病例有明確家族史,而絕大多數(shù)患者的發(fā)病原因仍然成謎。
更令人困惑的是,即使攜帶已知的致病基因突變,如SNCA或LRRK2基因變異,也并非所有人都會(huì)發(fā)病。這種不完全外顯現(xiàn)象提示我們,遺傳因素 alone 并不足以引發(fā)疾病。那么,是什么決定了攜帶易感基因的個(gè)體最終是否會(huì)發(fā)展為帕金森病患者?近年來,科學(xué)家們逐漸將目光投向基因與環(huán)境之間復(fù)雜的相互作用,而最新研究發(fā)現(xiàn),一組名為細(xì)胞色素P450的酶系可能在這一過程中扮演著關(guān)鍵角色。

圖1 帕金森病病因?qū)W的多維視角
在這篇發(fā)表于《npj Parkinson's Disease》的視角文章中,研究人員提出了一個(gè)全新的多維框架來理解帕金森病的病因。他們通過系統(tǒng)分析帕金森病標(biāo)志物計(jì)劃(PPMI)數(shù)據(jù)庫中的基因組數(shù)據(jù),發(fā)現(xiàn)細(xì)胞色素P450酶系與帕金森病發(fā)病風(fēng)險(xiǎn)存在顯著關(guān)聯(lián)。這些酶不僅參與外源性毒素的代謝,還調(diào)控著體內(nèi)膽固醇降解、維生素代謝以及類二十烷酸等重要生理過程,恰如連接遺傳易感性與環(huán)境因素的重要橋梁。
研究人員采用全基因組關(guān)聯(lián)分析(GWAS)方法,系統(tǒng)篩查了57種人類P450酶及其三個(gè)氧化還原伴侶基因中的單核苷酸多態(tài)性(SNP)。結(jié)果顯示,與健康對(duì)照組相比,PD患者在26種P450酶基因中存在顯著的變異富集現(xiàn)象( odds ratios 顯示5-10倍的富集度),這些變異主要分布在基因的調(diào)控區(qū)域。特別值得注意的是,參與毒素降解的P450亞型(如CYP2D6)在PD患者中表現(xiàn)出明顯的變異模式,這與環(huán)境毒素在PD病因中的作用高度一致。
研究還發(fā)現(xiàn),P450基因變異可能成為決定遺傳易感個(gè)體是否發(fā)病的“第二擊”。對(duì)攜帶已知PD基因突變(如LRRK2或GBA1)的個(gè)體進(jìn)行分析時(shí)發(fā)現(xiàn),從無癥狀狀態(tài)發(fā)展為臨床患者(GUN→GPD)的過程中,往往伴隨著P450基因的額外變異。三種代謝通路被證實(shí)尤為關(guān)鍵:維生素A和D代謝、膽固醇降解以及脂肪酸/類二十烷酸代謝。例如,參與雌激素和維生素A代謝的CYP1B1新近被證實(shí)與PD相關(guān),而腦膽固醇降解關(guān)鍵酶CYP46A1的變異則可能成為治療干預(yù)的靶點(diǎn)。
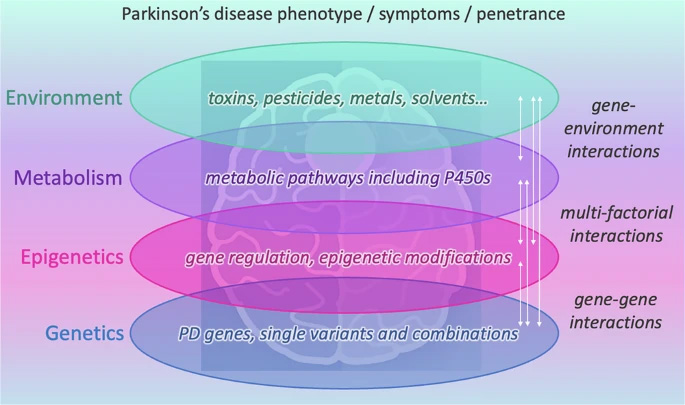
圖2 帕金森病的表型/癥狀/外顯率
研究的關(guān)鍵技術(shù)方法包括基于PPMI數(shù)據(jù)庫的大規(guī)?;蚪M數(shù)據(jù)分析、全基因組關(guān)聯(lián)研究(GWAS)篩選P450酶系單核苷酸多態(tài)性(SNP)、病例-對(duì)照研究設(shè)計(jì)比較PD患者與健康人群的基因變異頻率,以及利用 odds ratios 計(jì)算評(píng)估變異富集程度。
Cytochrome P450 enzymes as emerging contributors to the etiology of PD
研究發(fā)現(xiàn)P450酶系通過多重機(jī)制參與PD發(fā)?。菏紫?,它們負(fù)責(zé)降解環(huán)境毒素(如農(nóng)藥),基因變異可能導(dǎo)致解毒功能受損;其次,它們調(diào)控腦內(nèi)膽固醇穩(wěn)態(tài)和維生素代謝,這些過程的紊亂與神經(jīng)炎癥和神經(jīng)元死亡密切相關(guān)。特別值得注意的是,某些P450基因的變異頻率與已知PD風(fēng)險(xiǎn)基因GBA1處于同一數(shù)量級(jí),提示其臨床重要性。
What are the consequences of these observations?
這一多維視角完美契合Braak的腸腦軸假說和雙重打擊假說,將炎癥反應(yīng)、遺傳易感性、環(huán)境毒素暴露和衰老過程整合統(tǒng)一。研究表明單一因素很少足以引發(fā)PD,而是需要多個(gè)打擊的共同作用,這解釋了疾病表現(xiàn)的異質(zhì)性和治療反應(yīng)的差異性。
Novel and future possibilities to causatively treat PD
基于P450酶系在PD中的新角色,研究人員提出個(gè)性化治療新策略:針對(duì)特定代謝通路缺陷進(jìn)行干預(yù),如維生素D代謝異常者補(bǔ)充維生素D或抑制其降解;利用已知P450抑制劑(如他汀類藥物)調(diào)整膽固醇代謝;對(duì)毒素暴露高風(fēng)險(xiǎn)人群進(jìn)行基因篩查和預(yù)防性保護(hù)。全基因組測(cè)序與人工智能結(jié)合將成為發(fā)現(xiàn)個(gè)體化治療靶點(diǎn)的關(guān)鍵工具。
這項(xiàng)研究的重大意義在于突破了傳統(tǒng)單因素病因觀的局限,建立了帕金森病發(fā)病機(jī)制的多維整合模型。細(xì)胞色素P450酶系的發(fā)現(xiàn)為理解基因-環(huán)境交互作用提供了分子橋梁,為開發(fā)真正意義上的個(gè)性化治療奠定了理論基礎(chǔ)。未來,基于患者特異的基因變異組合、環(huán)境暴露史和代謝特征,醫(yī)生可能制定出更加精準(zhǔn)的防治策略,最終延緩甚至阻止這一重大腦疾病的進(jìn)展。
參考資料
[1] A multi-dimensional view on the etiology of Parkinson’s disease
摘要:本研究突破傳統(tǒng)單因素病因框架,提出帕金森病(PD)的多維度發(fā)病機(jī)制。
當(dāng)談及帕金森病,人們往往會(huì)想到震顫、行動(dòng)遲緩等運(yùn)動(dòng)癥狀,但隱藏在這些表象之下的病因之謎卻一直困擾著科學(xué)界。這種神經(jīng)退行性疾病已成為全球增長最快的神經(jīng)系統(tǒng)疾病,預(yù)計(jì)到2040年患者人數(shù)將達(dá)到1750萬。傳統(tǒng)上,醫(yī)學(xué)界將帕金森病劃分為家族性和散發(fā)性兩種類型,然而這種非黑即白的分類方式正面臨挑戰(zhàn)——僅有10-15%的病例有明確家族史,而絕大多數(shù)患者的發(fā)病原因仍然成謎。
更令人困惑的是,即使攜帶已知的致病基因突變,如SNCA或LRRK2基因變異,也并非所有人都會(huì)發(fā)病。這種不完全外顯現(xiàn)象提示我們,遺傳因素 alone 并不足以引發(fā)疾病。那么,是什么決定了攜帶易感基因的個(gè)體最終是否會(huì)發(fā)展為帕金森病患者?近年來,科學(xué)家們逐漸將目光投向基因與環(huán)境之間復(fù)雜的相互作用,而最新研究發(fā)現(xiàn),一組名為細(xì)胞色素P450的酶系可能在這一過程中扮演著關(guān)鍵角色。

圖1 帕金森病病因?qū)W的多維視角
在這篇發(fā)表于《npj Parkinson's Disease》的視角文章中,研究人員提出了一個(gè)全新的多維框架來理解帕金森病的病因。他們通過系統(tǒng)分析帕金森病標(biāo)志物計(jì)劃(PPMI)數(shù)據(jù)庫中的基因組數(shù)據(jù),發(fā)現(xiàn)細(xì)胞色素P450酶系與帕金森病發(fā)病風(fēng)險(xiǎn)存在顯著關(guān)聯(lián)。這些酶不僅參與外源性毒素的代謝,還調(diào)控著體內(nèi)膽固醇降解、維生素代謝以及類二十烷酸等重要生理過程,恰如連接遺傳易感性與環(huán)境因素的重要橋梁。
研究人員采用全基因組關(guān)聯(lián)分析(GWAS)方法,系統(tǒng)篩查了57種人類P450酶及其三個(gè)氧化還原伴侶基因中的單核苷酸多態(tài)性(SNP)。結(jié)果顯示,與健康對(duì)照組相比,PD患者在26種P450酶基因中存在顯著的變異富集現(xiàn)象( odds ratios 顯示5-10倍的富集度),這些變異主要分布在基因的調(diào)控區(qū)域。特別值得注意的是,參與毒素降解的P450亞型(如CYP2D6)在PD患者中表現(xiàn)出明顯的變異模式,這與環(huán)境毒素在PD病因中的作用高度一致。
研究還發(fā)現(xiàn),P450基因變異可能成為決定遺傳易感個(gè)體是否發(fā)病的“第二擊”。對(duì)攜帶已知PD基因突變(如LRRK2或GBA1)的個(gè)體進(jìn)行分析時(shí)發(fā)現(xiàn),從無癥狀狀態(tài)發(fā)展為臨床患者(GUN→GPD)的過程中,往往伴隨著P450基因的額外變異。三種代謝通路被證實(shí)尤為關(guān)鍵:維生素A和D代謝、膽固醇降解以及脂肪酸/類二十烷酸代謝。例如,參與雌激素和維生素A代謝的CYP1B1新近被證實(shí)與PD相關(guān),而腦膽固醇降解關(guān)鍵酶CYP46A1的變異則可能成為治療干預(yù)的靶點(diǎn)。

圖2 帕金森病的表型/癥狀/外顯率
研究的關(guān)鍵技術(shù)方法包括基于PPMI數(shù)據(jù)庫的大規(guī)?;蚪M數(shù)據(jù)分析、全基因組關(guān)聯(lián)研究(GWAS)篩選P450酶系單核苷酸多態(tài)性(SNP)、病例-對(duì)照研究設(shè)計(jì)比較PD患者與健康人群的基因變異頻率,以及利用 odds ratios 計(jì)算評(píng)估變異富集程度。
Cytochrome P450 enzymes as emerging contributors to the etiology of PD
研究發(fā)現(xiàn)P450酶系通過多重機(jī)制參與PD發(fā)?。菏紫?,它們負(fù)責(zé)降解環(huán)境毒素(如農(nóng)藥),基因變異可能導(dǎo)致解毒功能受損;其次,它們調(diào)控腦內(nèi)膽固醇穩(wěn)態(tài)和維生素代謝,這些過程的紊亂與神經(jīng)炎癥和神經(jīng)元死亡密切相關(guān)。特別值得注意的是,某些P450基因的變異頻率與已知PD風(fēng)險(xiǎn)基因GBA1處于同一數(shù)量級(jí),提示其臨床重要性。
What are the consequences of these observations?
這一多維視角完美契合Braak的腸腦軸假說和雙重打擊假說,將炎癥反應(yīng)、遺傳易感性、環(huán)境毒素暴露和衰老過程整合統(tǒng)一。研究表明單一因素很少足以引發(fā)PD,而是需要多個(gè)打擊的共同作用,這解釋了疾病表現(xiàn)的異質(zhì)性和治療反應(yīng)的差異性。
Novel and future possibilities to causatively treat PD
基于P450酶系在PD中的新角色,研究人員提出個(gè)性化治療新策略:針對(duì)特定代謝通路缺陷進(jìn)行干預(yù),如維生素D代謝異常者補(bǔ)充維生素D或抑制其降解;利用已知P450抑制劑(如他汀類藥物)調(diào)整膽固醇代謝;對(duì)毒素暴露高風(fēng)險(xiǎn)人群進(jìn)行基因篩查和預(yù)防性保護(hù)。全基因組測(cè)序與人工智能結(jié)合將成為發(fā)現(xiàn)個(gè)體化治療靶點(diǎn)的關(guān)鍵工具。
這項(xiàng)研究的重大意義在于突破了傳統(tǒng)單因素病因觀的局限,建立了帕金森病發(fā)病機(jī)制的多維整合模型。細(xì)胞色素P450酶系的發(fā)現(xiàn)為理解基因-環(huán)境交互作用提供了分子橋梁,為開發(fā)真正意義上的個(gè)性化治療奠定了理論基礎(chǔ)。未來,基于患者特異的基因變異組合、環(huán)境暴露史和代謝特征,醫(yī)生可能制定出更加精準(zhǔn)的防治策略,最終延緩甚至阻止這一重大腦疾病的進(jìn)展。
參考資料
[1] A multi-dimensional view on the etiology of Parkinson’s disease



