摘要:研究表明,信使RNA上常見的一種微小的化學(xué)修飾在細(xì)胞對壓力的反應(yīng)中發(fā)揮了令人驚訝的巨大作用。
一種在信使核糖核酸(mRNA)上常見的微小化學(xué)修飾,在細(xì)胞應(yīng)對壓力的過程中發(fā)揮著意想不到的巨大作用。這一發(fā)現(xiàn)闡明了細(xì)胞生物學(xué)的一個重要方面,并且可能具有臨床意義,因?yàn)檫@種被稱為m6A的mRNA修飾是新興癌癥治療類別中的靶點(diǎn)。
信使核糖核酸(mRNA)是攜帶制造蛋白質(zhì)的遺傳指令的分子,通常帶有m6A修飾,這種化學(xué)修飾就像一個“丟棄標(biāo)簽”。細(xì)胞存活和其他應(yīng)激反應(yīng)相關(guān)的mRNA往往比普通mRNA含有更多的m6A修飾。在正常情況下,這個標(biāo)簽有助于分解這些mRNA,使應(yīng)激反應(yīng)蛋白保持在低水平。
 圖1 mRNA上的N6-甲基腺苷通過促進(jìn)相分離核體的形成抑制髓系白血病分化
圖1 mRNA上的N6-甲基腺苷通過促進(jìn)相分離核體的形成抑制髓系白血病分化在這項(xiàng)于5月5日發(fā)表在《細(xì)胞》雜志上的研究中,研究人員揭示了這一過程的驚人細(xì)節(jié)。他們發(fā)現(xiàn),m6A觸發(fā)mRNA的分解過程,而這一過程發(fā)生在核糖體讀取mRNA的同時,核糖體是將mRNA中的指令轉(zhuǎn)化為特定蛋白質(zhì)的細(xì)胞機(jī)器。他們發(fā)現(xiàn)核糖體不僅僅是讀取mRNA,還會在分子上搜尋m6A修飾,并確保帶有這種修飾的mRNA被靶向降解。然后,科學(xué)家們發(fā)現(xiàn),當(dāng)細(xì)胞受到壓力時,這種分解過程會被暫停,從而使應(yīng)激反應(yīng)mRNA得以積累并產(chǎn)生幫助細(xì)胞恢復(fù)的蛋白質(zhì)。
“這些發(fā)現(xiàn)以一種將改變我們對應(yīng)激反應(yīng)和癌癥中m6A作用的看法的方式,回答了關(guān)于m6A的基本問題,”該研究的資深作者、威爾·康奈爾醫(yī)學(xué)院藥理學(xué)系的Greenberg-Starr教授、桑德拉和愛德華·邁耶癌癥中心成員Samie Jaffrey博士說。
自20世紀(jì)70年代以來,人們就知道信使核糖核酸常含有m6A,但這一修飾在過去幾年才開始受到關(guān)注,許多重要問題仍未解決。
“我們知道信使核糖核酸上的m6A存在可以誘導(dǎo)其降解,但我們之前并不知道m(xù)6A對mRNA的強(qiáng)效降解作用是開啟和關(guān)閉的,以此來控制細(xì)胞生理?!痹撗芯康谝蛔髡摺⑼枴た的螤栣t(yī)學(xué)院藥理學(xué)講師Shino Murakami博士說。
研究人員最初懷疑在細(xì)胞應(yīng)激時,一定有某種細(xì)胞途徑關(guān)閉了m6A的降解作用。為了找到這個關(guān)閉開關(guān),研究人員查閱了一個詳盡的公共數(shù)據(jù)庫,該數(shù)據(jù)庫記錄了細(xì)胞在接觸多種不同類型的化學(xué)物質(zhì)和處理后mRNA水平的變化。他們發(fā)現(xiàn),接觸抑制核糖體化合物的細(xì)胞中,通常含量較低的含有m6A的信使核糖核酸水平異常高。這表明核糖體參與了帶有m6A的mRNA的降解過程。
這一認(rèn)識引導(dǎo)他們發(fā)現(xiàn)了一系列意外的事件:他們發(fā)現(xiàn),當(dāng)核糖體在信使核糖核酸上遇到m6A時,會基本停止移動。在正常細(xì)胞條件下,另一個核糖體可能在同一RNA上移動,甚至在第一個核糖體剛要經(jīng)過m6A時就已到達(dá)此處,導(dǎo)致兩個核糖體發(fā)生碰撞。這些“意外事故”實(shí)際上是有意義的事件,它們會吸引能夠讀取m6A的蛋白質(zhì),從而啟動RNA的分解。通過這種方式,由帶有m6A修飾的mRNA編碼的應(yīng)激反應(yīng)蛋白在正常、非應(yīng)激條件下大多被阻止產(chǎn)生。
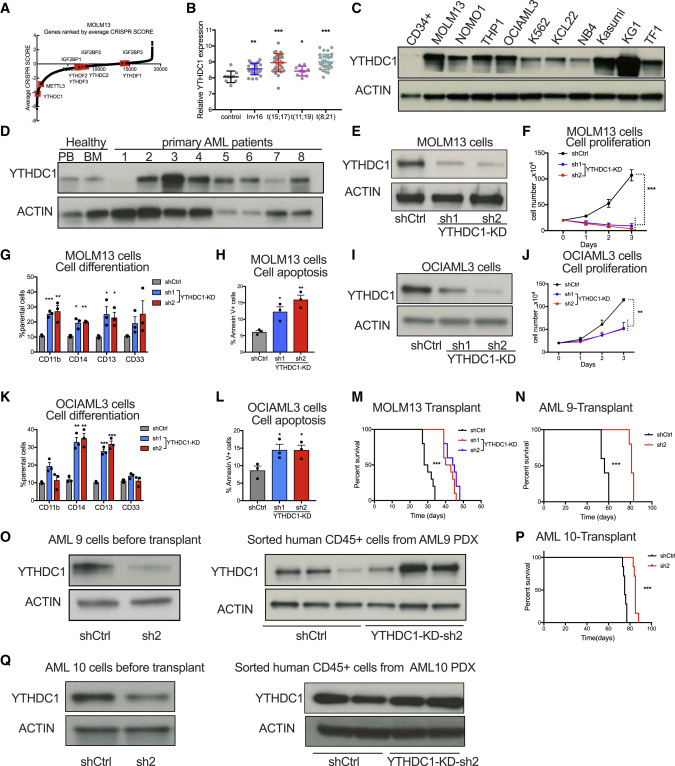
圖2 YTHDC1是白血病細(xì)胞存活所必需的
另一方面,在細(xì)胞應(yīng)激期間,核糖體活動通常會減少,因此可供發(fā)生碰撞的核糖體數(shù)量減少。因此,含有m6A的mRNA得以積累并轉(zhuǎn)化為應(yīng)激反應(yīng)蛋白。
Jaffrey博士說:“m6A途徑通常有助于抑制細(xì)胞的應(yīng)激反應(yīng),但我們知道在細(xì)胞應(yīng)激時一定有一個開關(guān)將其關(guān)閉,而核糖體是這個開關(guān)的關(guān)鍵要素?!?
這項(xiàng)發(fā)現(xiàn)可能對癌癥治療具有啟示意義。新興的抗m6A療法通過抑制催化m6A在mRNA上形成的酶METTL3,正在進(jìn)行臨床試驗(yàn)。這項(xiàng)研究提出了這些藥物可能通過誘導(dǎo)應(yīng)激反應(yīng)蛋白的表達(dá)來發(fā)揮作用的可能性,而應(yīng)激反應(yīng)蛋白已知可以抑制某些癌細(xì)胞的生長。
Jaffrey博士說:“我們的新發(fā)現(xiàn)為預(yù)測哪些類型的癌癥將對應(yīng)METTL3抑制劑提供了策略,這可以幫助我們識別出將對該療法反應(yīng)最佳的患者。”
參考資料
[1] N6-Methyladenosine on mRNA facilitates a phase-separated nuclear body that suppresses myeloid leukemic differentiation
摘要:研究表明,信使RNA上常見的一種微小的化學(xué)修飾在細(xì)胞對壓力的反應(yīng)中發(fā)揮了令人驚訝的巨大作用。
一種在信使核糖核酸(mRNA)上常見的微小化學(xué)修飾,在細(xì)胞應(yīng)對壓力的過程中發(fā)揮著意想不到的巨大作用。這一發(fā)現(xiàn)闡明了細(xì)胞生物學(xué)的一個重要方面,并且可能具有臨床意義,因?yàn)檫@種被稱為m6A的mRNA修飾是新興癌癥治療類別中的靶點(diǎn)。
信使核糖核酸(mRNA)是攜帶制造蛋白質(zhì)的遺傳指令的分子,通常帶有m6A修飾,這種化學(xué)修飾就像一個“丟棄標(biāo)簽”。細(xì)胞存活和其他應(yīng)激反應(yīng)相關(guān)的mRNA往往比普通mRNA含有更多的m6A修飾。在正常情況下,這個標(biāo)簽有助于分解這些mRNA,使應(yīng)激反應(yīng)蛋白保持在低水平。
 圖1 mRNA上的N6-甲基腺苷通過促進(jìn)相分離核體的形成抑制髓系白血病分化
圖1 mRNA上的N6-甲基腺苷通過促進(jìn)相分離核體的形成抑制髓系白血病分化在這項(xiàng)于5月5日發(fā)表在《細(xì)胞》雜志上的研究中,研究人員揭示了這一過程的驚人細(xì)節(jié)。他們發(fā)現(xiàn),m6A觸發(fā)mRNA的分解過程,而這一過程發(fā)生在核糖體讀取mRNA的同時,核糖體是將mRNA中的指令轉(zhuǎn)化為特定蛋白質(zhì)的細(xì)胞機(jī)器。他們發(fā)現(xiàn)核糖體不僅僅是讀取mRNA,還會在分子上搜尋m6A修飾,并確保帶有這種修飾的mRNA被靶向降解。然后,科學(xué)家們發(fā)現(xiàn),當(dāng)細(xì)胞受到壓力時,這種分解過程會被暫停,從而使應(yīng)激反應(yīng)mRNA得以積累并產(chǎn)生幫助細(xì)胞恢復(fù)的蛋白質(zhì)。
“這些發(fā)現(xiàn)以一種將改變我們對應(yīng)激反應(yīng)和癌癥中m6A作用的看法的方式,回答了關(guān)于m6A的基本問題,”該研究的資深作者、威爾·康奈爾醫(yī)學(xué)院藥理學(xué)系的Greenberg-Starr教授、桑德拉和愛德華·邁耶癌癥中心成員Samie Jaffrey博士說。
自20世紀(jì)70年代以來,人們就知道信使核糖核酸常含有m6A,但這一修飾在過去幾年才開始受到關(guān)注,許多重要問題仍未解決。
“我們知道信使核糖核酸上的m6A存在可以誘導(dǎo)其降解,但我們之前并不知道m(xù)6A對mRNA的強(qiáng)效降解作用是開啟和關(guān)閉的,以此來控制細(xì)胞生理?!痹撗芯康谝蛔髡?、威爾·康奈爾醫(yī)學(xué)院藥理學(xué)講師Shino Murakami博士說。
研究人員最初懷疑在細(xì)胞應(yīng)激時,一定有某種細(xì)胞途徑關(guān)閉了m6A的降解作用。為了找到這個關(guān)閉開關(guān),研究人員查閱了一個詳盡的公共數(shù)據(jù)庫,該數(shù)據(jù)庫記錄了細(xì)胞在接觸多種不同類型的化學(xué)物質(zhì)和處理后mRNA水平的變化。他們發(fā)現(xiàn),接觸抑制核糖體化合物的細(xì)胞中,通常含量較低的含有m6A的信使核糖核酸水平異常高。這表明核糖體參與了帶有m6A的mRNA的降解過程。
這一認(rèn)識引導(dǎo)他們發(fā)現(xiàn)了一系列意外的事件:他們發(fā)現(xiàn),當(dāng)核糖體在信使核糖核酸上遇到m6A時,會基本停止移動。在正常細(xì)胞條件下,另一個核糖體可能在同一RNA上移動,甚至在第一個核糖體剛要經(jīng)過m6A時就已到達(dá)此處,導(dǎo)致兩個核糖體發(fā)生碰撞。這些“意外事故”實(shí)際上是有意義的事件,它們會吸引能夠讀取m6A的蛋白質(zhì),從而啟動RNA的分解。通過這種方式,由帶有m6A修飾的mRNA編碼的應(yīng)激反應(yīng)蛋白在正常、非應(yīng)激條件下大多被阻止產(chǎn)生。

圖2 YTHDC1是白血病細(xì)胞存活所必需的
另一方面,在細(xì)胞應(yīng)激期間,核糖體活動通常會減少,因此可供發(fā)生碰撞的核糖體數(shù)量減少。因此,含有m6A的mRNA得以積累并轉(zhuǎn)化為應(yīng)激反應(yīng)蛋白。
Jaffrey博士說:“m6A途徑通常有助于抑制細(xì)胞的應(yīng)激反應(yīng),但我們知道在細(xì)胞應(yīng)激時一定有一個開關(guān)將其關(guān)閉,而核糖體是這個開關(guān)的關(guān)鍵要素?!?
這項(xiàng)發(fā)現(xiàn)可能對癌癥治療具有啟示意義。新興的抗m6A療法通過抑制催化m6A在mRNA上形成的酶METTL3,正在進(jìn)行臨床試驗(yàn)。這項(xiàng)研究提出了這些藥物可能通過誘導(dǎo)應(yīng)激反應(yīng)蛋白的表達(dá)來發(fā)揮作用的可能性,而應(yīng)激反應(yīng)蛋白已知可以抑制某些癌細(xì)胞的生長。
Jaffrey博士說:“我們的新發(fā)現(xiàn)為預(yù)測哪些類型的癌癥將對應(yīng)METTL3抑制劑提供了策略,這可以幫助我們識別出將對該療法反應(yīng)最佳的患者?!?/div>
參考資料
[1] N6-Methyladenosine on mRNA facilitates a phase-separated nuclear body that suppresses myeloid leukemic differentiation



